Neue Veröffentlichung in "Nature Communications"
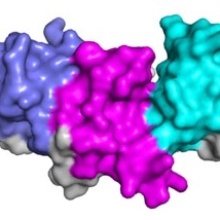
SETDB1 ist eine Histon-Methyltransferase, die H3K9me3-Markierungen in euchromatischen Regionen erzeugt. In Zusammenarbeit mit Wissenschaftlern von der Universität Toronto in Kanada zeigen wir hier, dass die Triple-Tudor-Domäne von SETDB1 Histon H3-Enden mit K14-Acetylierung in Kombination mit K9-Methylierung bindet, und dass die K9me/K14ac-Modifikation einen neuen bivalenten Chromatin-Status definiert. Strukturanalysen zeigten, dass Peptidbindung und K14ac-Erkennung an der Grenzfläche zwischen den Tudor-Domänen 2 und 3 auftreten. Bemerkenswerterweise wurde ein Taschenwechselmechanismus beobachtet, in dem K9me1 und K9me2 bevorzugt vom aromatischen Käfig von TD3 erkannt werden, während K9me3 selektiv an TD2 bindet. Genomische Analysen zeigen, dass K9me3/K14ac an SETDB1-Bindungsstellen mit LINE-Elementen angereichert ist, was darauf hindeutet, dass die Rekrutierung des SETDB1-Komplexes an K14ac/K9me-Regionen eine Rolle beim Silencing aktiver genomischer Regionen spielt.
| Kontakt | Prof. Dr. Albert Jeltsch |
|---|